PPT Scheikunde PowerPoint Presentation, free download ID4593308
Eerst geven we de definitie van een buffer. Daarna zullen we de verschillende kanten van de samenstelling van buffers en de berekening van de pH van bufferoplossingen bespreken. »»» Een buffer-oplossing is een oplossing waarvan de pH niet merkbaar verandert wanneer er water of kleine hoeveelheden zuur of base aan. Bijgewerkt op 04 mei 2019. Een buffer is een oplossing die ofwel een zwak zuur en zijn zout bevat, ofwel een zwakke base en zijn zout , die bestand is tegen veranderingen in pH . Met andere woorden, een buffer is een waterige oplossing van ofwel een zwak zuur en zijn geconjugeerde base of een zwakke base en zijn geconjugeerde zuur.

Buffers nhscrazy4chem

Scheikunde elektrolyse Elektrolyse Inleiding Elektrolyse is een chemische reactie die vaak

Chemisch rekenen Les 7 Buffers Chemisch rekenen Les 7 Buffers Een buffer bestaat uit een zwak

Wat is hydratatie? Havo vwo scheikunde (Kort) YouTube
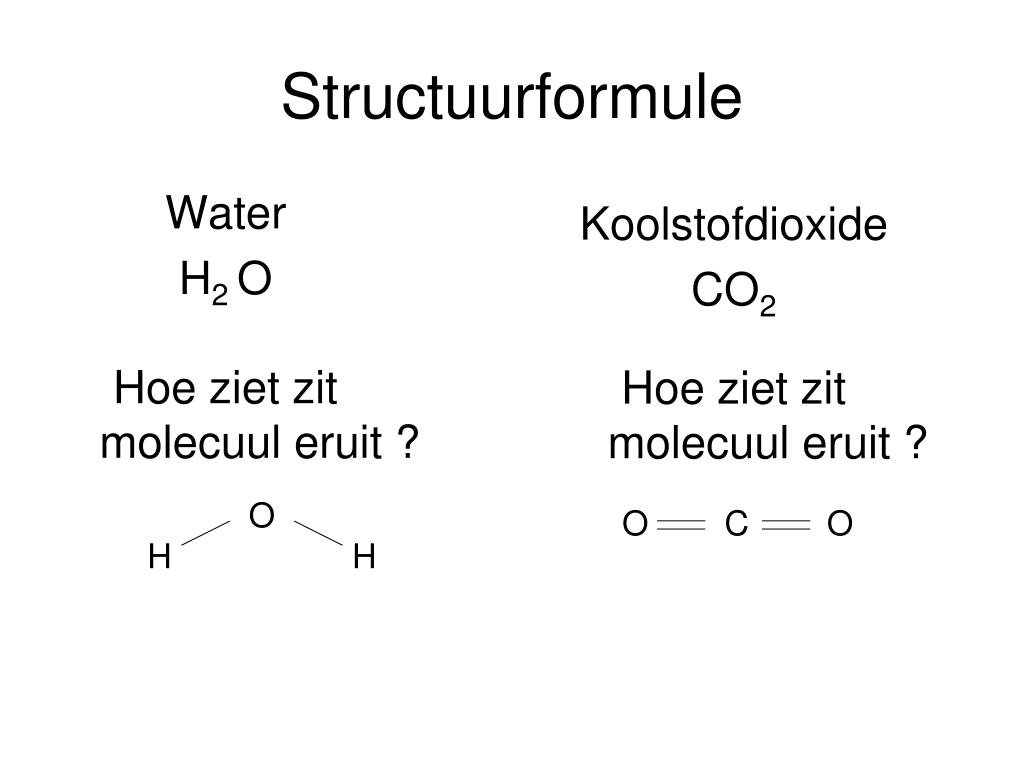
PPT Scheikunde PowerPoint Presentation, free download ID6136099

Basisch vs Zuur Ontzuren.info

Examen scheikunde Buffers (Zuren en basen) YouTube

Scheikunde en ik YouTube

PPT Scheikunde PowerPoint Presentation, free download ID4593308

Scheikunde blokjesschema BètaBijles Online
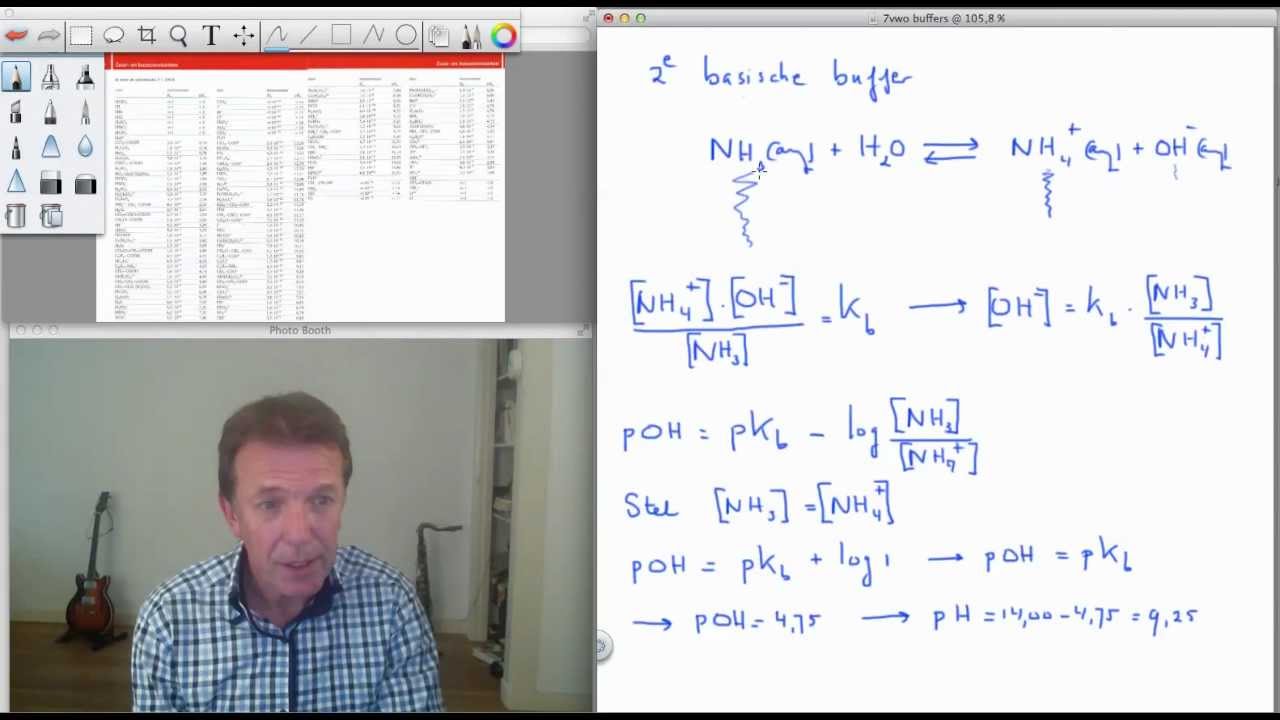
17 VWO Buffers scheikunde YouTube

Wat Is Een Zout In De Scheikunde Alles Wat Je Moet Weten

SO Scheikunde § 3

Scheikunde hoofdstuk 14 Het is de basis voor een groot aantal stoffen (ethanol, azijnzuur

Scheikunde buffer maken voorbeeldopgave YouTube

esters scheikunde YouTube

rendement bij scheikunde YouTube

Scheikunde proefvoorbereiding buffer Materiaal Labjas en bril Testvloeistof A (10 mL) 1,0 M
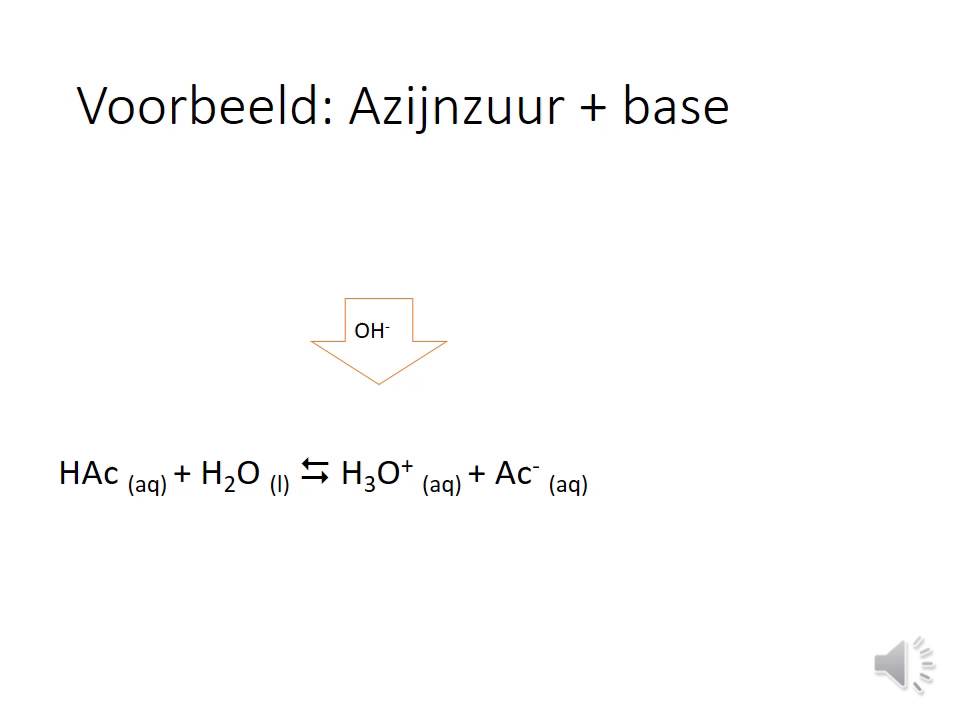
N3J2P2W5 2 Wat is een buffer YouTube

Aristotle a book on Science
buffer (scheikunde), een combinatie van stoffen die veranderingen in zuurgraad afremt. buffer (stootbalk), een uitsteeksel, vooral op railvoertuigen en doodlopende sporen, gewoonlijk per twee op een stootbalk. bufferzone, een (grond)gebied. bufferstaat, een staat die geheel in een bufferzone ligt, eventueel de bufferzone is.. Uitwerking: H2O NH3 We passen de bufferformule toe: pH pKz log n(NH3) 9,24 log 1 9,24 Vaak hebben we een buffer nodig met een bepaalde pH en willen we berekenen hoeveel zuur en base opgelost moet worden om buffer te maken. Uit het vorige voorbeeld blijkt dat de pH van een buffer gelijk is aan de pKz als de verhouding gelijk is aan 1.